Conjonctivites et dermatite atopique
Les patients atteints de dermatite atopique (DA) présentent un risque accru de pathologies de la surface oculaire (POS), la conjonctivite étant la plus fréquente de ces affections. La prise en compte de ces comorbidités ophtalmologiques a pris de l’importance depuis l’emploi des biothérapies bloquant la voie IL-4/IL-13 dont l’utilisation en condition réelle s’associe à des effets indésirables oculaires fréquents. Il est important qu’à la fois le dermatologue et le patient sachent évoquer leur diagnostic car elles peuvent entrainer des lésions invalidantes et parfois menacer la vue.
Pathologies oculaires de surface associées à la dermatite atopique
Les POS sont diagnostiquées chez 32 à 55 % des patients atteints de DA (1). Cette fréquence est probablement sous-estimée, plus proche en réalité de 90 %, puisque de nombreux patients ne signalent aucun symptômes (2). Elles sont d’autant plus fréquentes que la DA est sévère et touche le visage et/ou les paupières.
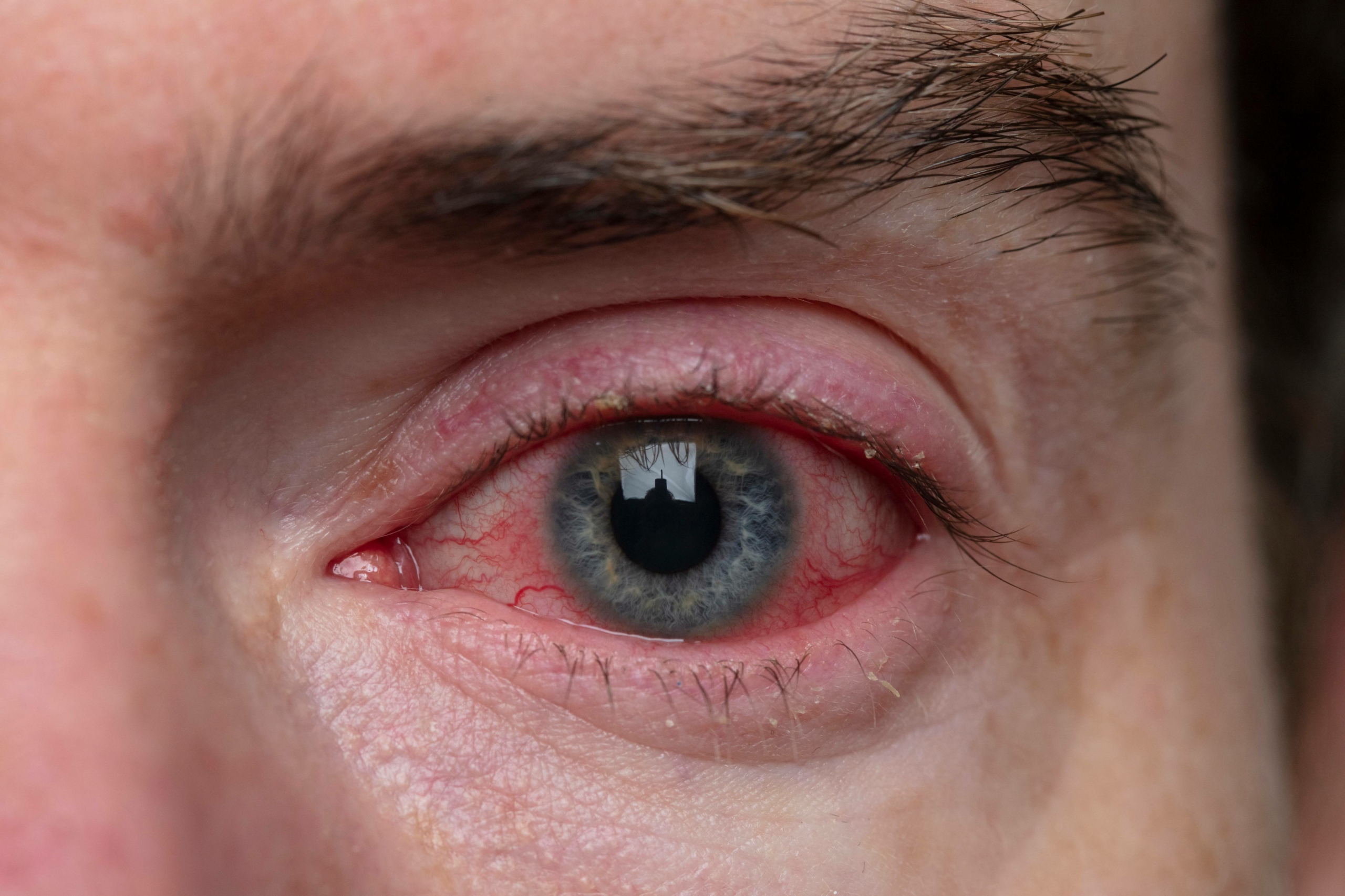
Parmi les POS, la conjonctivite apparait comme une inflammation de la conjonctive (palpébrale et bulbaire) avec des yeux rouges et larmoyants, une conjonctive enflée, des démangeaisons et une acuité visuelle normale. Il existe plusieurs sous-types de conjonctivites au cours de la DA : la conjonctivite saisonnière et pérenne (ou conjonctivite allergique), la blépharo-conjonctivite atopique (inflammation de la paupière et de la conjonctive environnante), la kératoconjonctivite vernale (inflammation chronique de la muqueuse oculaire) et la kératoconjonctivite atopique (KCA) (3).
La KCA est une maladie potentiellement menaçante pour la vue. Elle est parfois précédée d’une kérato-conjonctivite vernale à un plus jeune âge. On estime que 20 à 60% des patients atteints de DA vont développer une KCA. La KCA s’accompagne de larmes fréquentes, d’une sensation de corps étranger et souvent d’une photophobie. Les signes cliniques typiques sont une blépharite antérieure et postérieure avec un épaississement du bord de la paupière, une hyperémie conjonctivale, un épaississement et un écoulement mucoïde.
Les patients atteints de DA ont également un risque plus élevé de développer une conjonctivite bactérienne ou virale, les staphylocoques et les adénovirus étant respectivement les agents pathogènes les plus fréquents. Le virus de l’herpès simplex représente également une menace majeure pour la perte progressive de la vision dans la maladie atopique.
Conjonctivites sous biothérapie
La conjonctivite est l’événement indésirable le plus courant des essais de phase III des biothérapies anti IL-4/IL-13, avec une incidence plus marquée sous dupilumab (4.7 à 28 %) que sous tralokinumab (7.5 %) (4, 5). Deux facteurs accroissent le risque de conjonctivite sous dupilumab : la sévérité de la maladie et la préexistence d’une conjonctivite. Si les conjonctivites ainsi décrites dans les essais de ce étaient généralement légères et n’en nécessitaient que très rarement l’arrêt, il convient d’observer que, depuis sa commercialisation, a été signalé un nombre croissant de rapports de conjonctivites sévères induites par le dupilumab, nécessitant l’intervention d’un ophtalmologue. Ainsi, en condition réelle d’utilisation, l’incidence de la conjonctivite chez les patients traités par dupilumab est supérieure à celle des essais cliniques, estimée à 38.2% en France (6). Certains experts soulignent que ces chiffres plus importants se réfèrent à la plainte générale d’« yeux rouges et irrités » qui pourraient être non seulement en lien avec une conjonctivite mais aussi avec des yeux secs.
La survenue de conjonctivites sous biothérapie pourrait être en lien avec une altération de l’homéostasie conjonctivale par blocage des cytokines IL-4/IL-13 qui provoque une raréfaction des cellules caliciformes et une diminution de la sécrétion de mucine (1, 4).
Prévention et traitement de la conjonctivite sous biothérapie anti IL-4/IL-13
En cas d’antécédent de conjonctivite, une évaluation ophtalmologique initiale avant biothérapie est recommandée (7). Cette recommandation est cependant inapplicable la plupart du temps, tant l’attente pour un examen ophtalmologique est très longue et risque de retarder le traitement.
Dans tous les cas, le dermatologue doit informer ses patients des éventuels effets secondaires oculaires avant l’instauration d’une biothérapie afin de l’aider à identifier les symptômes. La conjonctivite doit être envisagée en cas de démangeaisons, d’une rougeur/hyperhémie, très souvent associées à des larmes et paupières enflées (blépharite). Le recours urgent à un ophtalmologiste est requis dans les situations suivantes : baisse de l’acuité visuelle, rougeur intense près de la cornée, douleur et photophobie. L’information du patient comporte également des mesures préventives (Tableau 1) (1, 7).
En cas de suspicion de conjonctivite sous biothérapie, la prescription comporte des larmes artificielles, un collyre antiallergique, du tacrolimus sur les paupières en cas de blépharite associée. La prescription d’un collyre stéroïdien est réservée à l’ophtalmologiste car non sans risque (aggravation de la kératite herpétique, glaucome). La poursuite de la biothérapie est autorisée. Le changement au profit d’une autre biothérapie (remplacement du dupilumab par tralokinumab par exemple) n’a pas démontré de manière irréfutable une amélioration des symptômes. En l’absence d’amélioration, un avis ophtalmologiste est recommandé pour adapter le traitement : corticostéroïdes en collyre, ciclosporine en gouttes, tacrolimus collyre oculaire voir application direct de tacrolimus dans les culs de sac conjonctivaux (8).
Auteur : Pr Guillaume Chaby, Service de Dermatologie CHU Amiens
Date : 28/11/2024
Références :
- Thyssen JP, Toft PB, Halling-Overgaard AS, et al. Incidence, prevalence, and risk of selected ocular disease in adults with atopic dermatitis. J Am Acad Dermatol 2017; 77: 280-6.
- Achten RE, Bakker DS, van Luijk CM, et al. Ocular surface disease is common in moderate-to-severe atopic dermatitis patients. Clin Exp Allergy 2022; 52: 801-5.
- Azari AA, Arabi A. Conjunctivitis: a systematic review. J Ophthalmic Vis Res 2020; 15: 372-95.
- Akinlade B, Guttman-Yassky E, de Bruin-Weller M, et al. Conjunctivitis in dupilumab clinical trials. Br J Dermatol 2019; 181: 436-7.
- Wollenberg A, Beck LA, de Bruin Weller M, et al. Conjunctivitis in adult patients with moderate-to-severe atopic dermatitis: results from five tralokinumab clinical trials. Br J Dermatol 2022; 186: 391-2.
- Faiz S, Giovannelli J, Podevin C, et al. Effectiveness and safety of dupilumab for the treatment of atopic dermatitis in a real-life French multicenter adult cohort. J Am Acad Dermatol 2019; 81: 143-51.
- Doan S, Arnould L, Febvay C, et al. Dupilumab-related blepharoconjunctivitis: Recommendations of the CEDRE group. J Fr Ophtalmol 2022; 45: 277-87.
- Shi VY, Chamberlain W, Siegfried E, et al. Practical management of ocular surface disease in patients with atopic dermatitis, with a focus on conjunctivitis: A review. J Am Acad Dermatol 2023; 89: 309-15.